
对于(yú)数百(bǎi)万患有癫痫(xián)症和帕金森病等运(yùn)动障碍的(de)人(rén)来说(shuō),脑的(de)电(diàn)刺激已经扩(kuò)大了治疗的可能性。未来(lái),电(diàn)刺激可能会帮(bāng)助患(huàn)有精(jīng)神(shén)疾病和直接(jiē)脑损伤(如卒(zú)中)的人。

梅奥诊所官网9月3日消息
然而(ér),研究大脑网络如何(hé)相互作用(yòng)是很(hěn)复(fù)杂的。可以(yǐ)通过在患者大脑的一个区域提供短暂(zàn)的电流脉(mò)冲同时测量其他区(qū)域的电压响应来探索大脑网络。原则上(shàng),人们(men)应该能够从这些数据中推断(duàn)出大脑网络的结(jié)构。然而(ér),对于真(zhēn)实世界的(de)数据,这(zhè)个问(wèn)题很困(kùn)难(nán),因为记录的信号很复杂(zá),并且可以进(jìn)行测(cè)量的(de)非(fēi)常有限。
为了使(shǐ)问题易于管理(lǐ),梅奥诊所(Mayo Clinic)的研究人(rén)员开发了一套范例或观点,以简(jiǎn)化电刺激对大脑影响之间(jiān)的比(bǐ)较。由于科学文献(xiàn)中(zhōng)不存在表(biǎo)征输入集合如(rú)何在人类大(dà)脑区(qū)域中融合的数学技术,因此 Mayo 团队与(yǔ)人工智能 (AI) 算法领域的国(guó)际专家合作开发了(le)一(yī)种称为“基(jī)本(běn)轮廓曲线识别”的新型算(suàn)法。”
在《PLOS 计算生物学》(PLOS Computational Biology)杂志上发表的这项研(yán)究中,一名脑肿(zhǒng)瘤患者在(zài)切除肿瘤之前接受了皮层电图(tú)(ECoG)电极阵列的放置,以定位癫痫发作(zuò)并绘制大(dà)脑功能图(tú)。每次电极相互(hù)作用都会导致使(shǐ)用新算法研(yán)究(jiū)数百到数千个时间点(diǎn)。

研(yán)究于2021年(nián)9月2日发表在《PLOS Computational Biology》(最(zuì)新影响因子:4.475)杂志上
“我们的研究结果表明,这种(zhǒng)新(xīn)型算法可以帮助我们了解哪些大脑区域直接相互交互,这反过来(lái)又可以帮助指导(dǎo)电(diàn)极(jí)的放置,以用于治疗脑部(bù)疾病网络的刺激设备,” 该研究的(de)第一作者、梅奥(ào)诊所神(shén)经外科医生(shēng)、医学博士 Kai Miller 说(shuō)。

Kai Miller 医生
“随着新技术的出现,这种(zhǒng)算法可能会帮助我(wǒ)们更(gèng)好地治疗癫痫、帕金(jīn)森病等运动障(zhàng)碍以及强迫症和抑(yì)郁症等精神(shén)疾病患者。”
“迄今为止,神经系(xì)统数据可(kě)能是人工智能研究人员建模时最具挑(tiāo)战性和最令(lìng)人兴奋的数据,”研究合著者兼 Google Research Brain 团队(duì)成员(yuán) Klaus-Robert Mueller 博士(shì)说。Mueller 博士是柏林学(xué)习和数据基础研究所(Berlin Institute for the Foundations of Learning and Data)的联合主任和(hé)机器学习小组(Machine Learning Group)的主(zhǔ)任, 研究(jiū)所(suǒ)和机器学习小组都在柏林技术大(dà)学(Technical University of Berlin)。
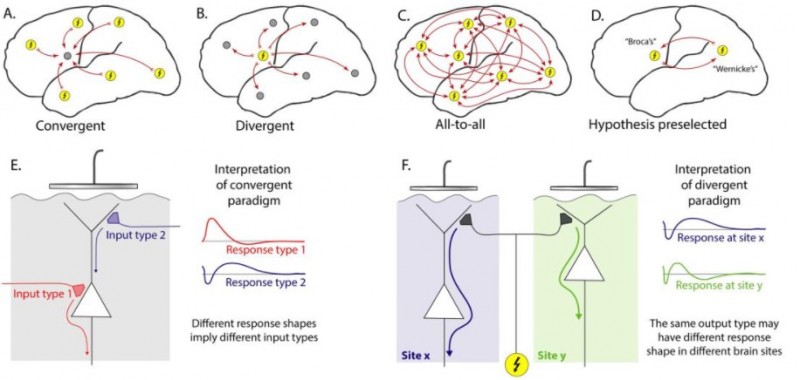
在这项研究中,作者提供了一个(gè)可下载(zǎi)的代码包,以便其(qí)他人可(kě)以(yǐ)探索该技(jì)术。“共享开发的代码是(shì)我们帮助研(yán)究可重复性努力的(de)核心部分(fèn),”梅奥诊所生物医学工程师(shī)和(hé)资深作(zuò)者 Dora Hermes 博(bó)士说。
















